Qui n’a pas consommé d’antibiotiques au moins une fois dans sa vie ? Ces médicaments qui servent à lutter contre diverses infections dues à des bactéries (pneumonies, bronchites, otites, méningites, infections urinaires, septicémies…) sauvent incontestablement des millions de vies. Mais leur efficacité est grandement menacée et « on risque à l’avenir de ne plus disposer d’antibiotiques permettant de soigner les infections bactériennes courantes », avertit l’Organisation mondiale de la santé (OMS).
Ces infections seraient de nouveau mortelles, et la société reviendrait à l’ère pré-antibiotique. Mourir d’une infection a priori « banale », car habituellement traitée facilement, est aujourd’hui possible dès lors qu’une bactérie devenue multirésistante aux antibiotiques est en cause… Déjà en Europe, 400 000 personnes sont infectées chaque année par de telles bactéries, dont 25 000 décèdent. Et l’augmentation de la résistance sera responsable d’une augmentation dramatique de ces chiffres comme cela a été modélisé dans le rapport de Lord J. O’Neil sur l’impact de la résistance aux antibiotiques d’ici 2050.
LES ANTIBIOTIQUES UTILISÉS DÈS LES ANNÉES 1940
Pour bien comprendre l’alarmant problème de « l’antibiorésistance », commençons par le commencement. Le premier antibiotique – la pénicilline G – fut découvert en 1928 par le biologiste écossais Alexander Fleming mais ne fut utilisé qu’à partir de 1941 . Entre temps, une autre classe d’antibiotiques, les sulfamides, dont l’action fut mise en évidence par des pasteuriens fut largement utilisée et sauva des milliers de vie pendant la seconde guerre mondiale.
Aujourd’hui, 70 ans après le début de l’usage des antibiotiques, il en existe plus de 15 familles – qui diffèrent de par leur structure chimique et leur mode d’action contre les bactéries. Quant au problème de l’antibiorésistance, il fut soulevé par Fleming lui-même dès 1945. Il pressentait les risques liés à une mauvaise utilisation de la molécule qu’il avait découverte : « Cela aboutirait à ce que, au lieu d’éliminer l’infection, on apprenne aux microbes à résister à la pénicilline et à ce que ces microbes soient transmis d’un individu à l’autre, jusqu’à ce qu’ils en atteignent un chez qui ils provoqueraient une pneumonie ou une septicémie que la pénicilline ne pourrait guérir. »
LA FIN DE L’ÂGE D’OR DES ANTIBIOTIQUES
Cet avertissement ne fut pas pris en compte au départ et les antibiotiques ont été largement utilisés dès les années 40, armes magiques contribuant avec plusieurs vaccins à faire chuter drastiquement l’impact des maladies infectieuses bactériennes, tout du moins dans les pays industrialisés. Mais « l’âge d’or » des antibiotiques s’acheva, au début des années 90. On prit alors de plus en plus conscience du nombre inquiétant – et croissant – de bactéries devenues résistantes aux antibiotiques et du tarissement de la découverte de nouvelles molécules pour lutter contre les bactéries résistantes.
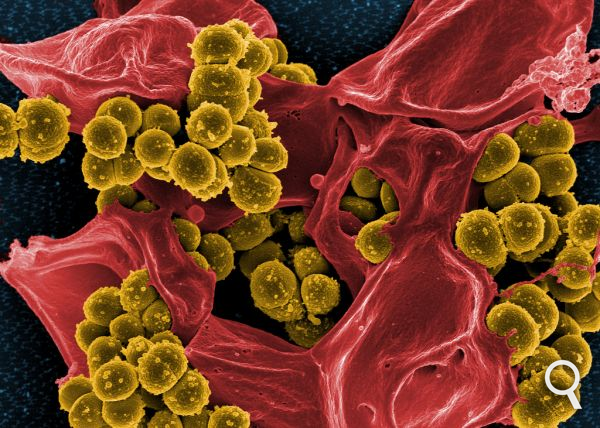
Des médecins se retrouvaient dans des situations d’impasse thérapeutique face à certains patients, aucun antibiotique n’ayant plus le moindre effet sur leur infection. Et le phénomène s’accélère. La situation est devenue particulièrement critique dans les hôpitaux, où l’on utilise – et c’est logique – beaucoup d’antibiotiques pour traiter les malades : la moitié des antibiotiques consommés en France en médecine humaine le sont à l’hôpital. Cette « pression » médicamenteuse provoque des résistances, et les bactéries résistantes passent aisément d’un individu à l’autre, qu’elles infectent d’autant plus facilement qu’il est affaibli. À l’hôpital, plus d’un staphylocoque doré sur cinq est résistant à la méticilline et à d’autres antibiotiques de la famille des pénicillines utilisés contre les infections qu’il provoque (pulmonaires, osseuses, septicémies…). De nombreux germes responsables d’infections acquises à l’hôpital – les infections nosocomiales – sont de plus en plus résistants à plusieurs antibiotiques.
BIENTÔT UNE PRÉOCCUPATION QUOTIDIENNE ?
Aujourd’hui, ces problèmes d’antibiorésisstance ne sont plus limités au seul milieu hospitalier et touchent les infections communautaires « en ville ». Sur les forums des sites médicaux, des personnes concernées s’interrogent, comme cette femme qui déclare : « Depuis six mois je fais des infections urinaires, toujours dues à un germe Escherichia coli résistant à de nombreux antibiotiques ». Elle énonce le nouveau traitement préconisé par son généraliste, basé sur un nouvel antibiotique, et questionne : « Ce germe très résistant ne va-t-il pas développer une plus grande résistance ? Qu’en pensez-vous ? » L’antibiorésistance est ainsi entrée dans les préoccupations quotidiennes de nombreux patients et inquiète bien entendu médecins et chercheurs.
« LES ANTIBIOTIQUES, C’EST PAS AUTOMATIQUE ! »
Les autorités de santé publique interviennent. Nous avons tous à l’esprit la campagne « Les antibiotiques, c’est pas automatique ! » lancée en 2002 par l’Assurance maladie. Elle visait à faire prendre conscience que les antibiotiques sont utiles exclusivement contre les infections provoquées par des bactéries et n’ont aucune efficacité contre les infections virales, à l’origine par exemple de nombreuses maladies hivernales (rhumes, certaines angines et bronchites, etc.). Et elle eut un net impact sur la consommation d’antibiotiques en France, qui diminua de 15 %. En 2010, une nouvelle campagne des pouvoirs publics s’attaquait plus directement au problème de la résistance aux antibiotiques en France avec pour slogan « si on les utilise à tort, ils deviendront moins forts ». Depuis l’Assurance maladie poursuit sa communication autour de la bonne utilisation des antibiotiques.
L’ESPOIR DES NANOMÉDICAMENTS ET LA QUÊTE DE NOUVEAUX ANTIBIOTIQUES
« Utiliser des nanoparticules – assemblages de sucres, de lipides ou de polymères– pour délivrer les antibiotiques pourrait permettre de les administrer à des doses inférieures, ou bien d’employer des antibiotiques aujourd’hui délaissés car mal tolérés », explique Brigitte Gicquel, responsable de l’unité de Génétique mycobactérienne à l’Institut Pasteur. Cette spécialiste de la tuberculose coordonne le projet européen NAREB*, lancé en février 2014, associant 14 laboratoires pour développer des nanomédicaments contre deux types d’infections très préoccupantes : celles dues au staphylocoque doré résistant à la méthicilline (SARM), cause fréquente d’infections nosocomiales sévères, et la tuberculose multirésistante. Les travaux du consortium NAREB ont montré pour un petit nombre d’antibiotiques la possibilité de les associer à des nanoparticules sans affecter leur activité in vitro et in vivo. Des travaux restent à faire pour démontrer la supériorité d’une association antibiotique/nanoparticule pour modifier les formulations actuellement utilisées.
Celle-ci représente actuellement 3,7 % des nouveaux cas de tuberculose dans le monde et 20 % des cas déjà traités, complexifiant une prise en charge déjà lourde pour une tuberculose « sensible » (plusieurs mois avec au moins 4 antibiotiques).
Sans compter que 84 pays ont déjà signalé à l’OMS des cas de tuberculose « ultrarésistante ». « Devant cette situation dramatique et le désengagement de la plupart du secteur industriel, nous, laboratoires académiques, devons faire un effort pour trouver de nouveaux antibiotiques et de nouvelles formulations », souligne Brigitte Gicquel, dont l’équipe participe activement à la recherche de nouveaux médicaments au sein de consortiums associant plusieurs instituts comme le projet NAREB. Nano ou nouveaux antibiotiques, le temps presse face à la résistance croissante du bacille de la tuberculose : cette maladie responsable d’un décès sur sept en Europe au XIXe siècle fait aujourd’hui plus de 8,5 millions de nouveaux malades et 1,3 million de morts chaque année dans le monde.
LIMITER LES DÉGÂTS
L’objectif aujourd’hui est bien de limiter la consommation d’antibiotiques pour freiner l’expansion de la résistance. Son émergence est un phénomène biologique naturel qui provient de la capacité qu’ont les bactéries à résister à une « attaque » par les antibiotiques, par le biais d’une mutation ou bien par l’acquisition de gènes de résistance provenant de bactéries déjà résistantes. Elle est bien sûr accélérée par l’utilisation et l’emploi abusif d’antibiotiques chez l’homme comme chez les animaux (voir encadré ci-dessous), qui consomment plus de 50 % des antibiotiques produits dans le monde d’après l’OMS. La grande difficulté est aussi de limiter la propagation des bactéries résistantes qui voyagent… avec l’Homme. Certaines ont particulièrement défrayé la chronique, comme ces diverses espèces bactériennes hébergeant le gène NDM-1 (de l’enzyme New Delhi métallo-beta-lactamase) leur conférant la résistance aux antibiotiques les plus récents, les carbapénèmes, réservés aux infections multirésistantes.
Elles avaient été détectées en 2009 chez un Suédois qui avait été hospitalisé en Inde et l’année suivante au Royaume-Uni, chez des personnes ayant fait du tourisme médical pour de la chirurgie esthétique en Inde ou au Pakistan.
L’AFFAIRE DE TOUS
Que faire face à ces risques majeurs ? « L’OMS appelle les principales parties prenantes, les décideurs et les planificateurs, le grand public et les patients, les praticiens et les prescripteurs, les pharmaciens et les dispensateurs, ainsi que l’industrie pharmaceutique, à agir et à prendre leurs responsabilités pour lutter contre la résistance aux antimicrobiens. » Si aujourd’hui la recherche doit se renforcer pour développer de nouveaux antibiotiques, le problème de la résistance bactérienne est bien l’affaire de tous, et donc de chacun d’entre nous, qui sommes invités à suivre quelques règles de base…
Source : Institut Pasteur
* Nanotherapeutics for antibiotic resistant emergent bacterial pathogens.